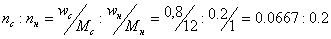|
|
|
|
|
|
|
|
|
Русская интерактивная дистанционная школа физики.
Открытые уроки. Учебники по физике. Задачи по физике. Справочник по физике. Единый государственный экзамен. Вопросы и консультации. Рефераты. Олимпиады и турниры. Современная физика. Веселая наука. Уголок крохобора. Не только физика. Директория ссылок. Репетиторы. Малая академия наук. . |
Разбор задач олимпиады по химии за 9 марта 2004. 1 Вовочка простудился, и у него поднялась температура 38. Во сколько раз скорость реакций в его организме стала выше, если температурный коэффициент реакций в Вовочке равен двум. У здорового Вовочки температура 36,6. Соотношение скоростей реакций в организме больного и здорового Вовочки определяется следующим образом: ut2/ut1=g(t2-t1)/10 g - температурный коэффициент реакций в Вовочке, t2 и t1 –его температура во время и после болезни. ut2/ut1=2(38-36.6)/10=20.14=1,102 Скорость реакций возрастет в 1,102 раза. 2 Вовочкина бабушка купила в гомеопатической аптеке лекарство. Оно содержало три компонента А В и С. Их концентрация составляла, если верить инструкции 10-15, 10-17 и 10-26 молей в литре (соответственно). С какой вероятностью в бабушкином флакончике есть все три компонента лекарства, если объем флакончика равен 20 мл. Для решения воспользуемся формулой N=CVNA, где N-число молекул в флаконе, C-молярная концентрация молекул, V-объем флакона в литрах, NA- число Авогадро. Тогда, для веществ A, B и C соответственно N(A)= 10-15?0,02?6,02?1023=1,2?107 N(B)= 10-17?0,02?6,02?1023=1,2?105 N(C)= 10-15?0,02?6,02?1023=1,2?10-4 Видно, что молекул веществ AиB в каждом флакончике много, а вот вещество С, попадется только каждой 1/N(A)=1/1,2?10-4=8333 ,бабушке. 3 Как диссоциируют растворимые в воде вещества (НОЭ* и НОЭ**) структурные формулы которых одинаковы: Н-О-Э. В веществе НОЭ* электроотрицательность Э* равна 0,97, а в НОЭ** равна 2,74. В веществе НОЭ* наиболее полярной является связь элемент – кислород т. к. разности электроотрицательностей равны DcН-О=3,5-2,1=1,4 а DcО-Э=3,5-0,97=2,53 Н-О-Э* диссоциирует как основание происходит разрыв наиболее полярной связи: Н-О-Э*® Н-О-+Э*+ реакция необратима, т. к. все растворимые основания (кроме NH4OH сильные). В веществе НОЭ** DcН-О=3,5-2,1=1,4 а DcО-Э=3,5-2,74=0,76 наиболее полярная связь Н-О, поэтому диссоциация идет по ней, т.е. НОЭ** диссоциирует как кислота НОЭ**« Н++О-Э** - кислота слабая и диссоциация обратима. Силу кислоты определяем по правилу Полинга: разность между числом атомов кислорода и водорода больше или равна 2-м – кислота сильная, меньше 2-х кислота слабая. 4 Углеводород имеет массовую долю атомов углерода 80% и плотность по метану 1,875, определить, что это за углеводород двумя способами, используя разные исходные данные. 1. Wc=0.8, Wн=1-0.8=0.2 Определим соотношение между числом молей
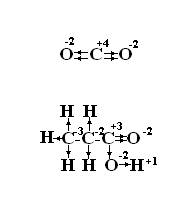
С и Н Таково соотношение между числом атомов углерода и водорода в молекуле искомого вещества. Разделим оба числа на наименьшее 0,0667 и получим простейшую формулу вещества С1H3 поскольку вещества с такой формулой не существует, умножим коэффициенты на 2 и помучим С2H6 – это этан. 2. Определим молярную массу вещества Допустим искомое вещество алкан, тогда его формула СnH2n+2, а его молярная масса равна 12n+2n+2 и равна 30 12n+2n+2=30 14n=28 n=2 т.к. n число атомов и мы получили целое число, это действительно алкан, а именно этан С2H6. 5 Уравнять реакции методом электронного баланса, предварительно определив степени окисления всех атомов в органических соединениях. C2H5NH2+O2®CO2+N2+H2O CH3-C? CH+KMnO4+H2SO4®CH3COOH+CO2+K2SO4+MnSO4+H2O. Самой сложной частью в этом задание является определение степеней окисления органических соединений. Можно предложить очень простой метод, для использования которого нужно знать структурную формулу соединения и иметь таблицу относительных электроотрицательностей. В структурной формуле вещества связи заменяем стрелками от менее электроотрицательного атома к более олектроотрицательному (двойные и тройные связи тоже), если электроотрицательности атомов равны стрелки не нужны. Затем считаем число стрелок вошедших и вышедших. Вошедшая стрелка дает минус в величину степени окисления, а вышедшая плюс. Покажем это на примере:
4C-3H3-C-1H2-N-3H2+15O2®8CO2+2N2+14H2O C-3-7e-®C+4 C-1-5e-®C+4 сумма отданных электронов 15 N-3-3e-®N0 O20+4e-®2O-2 принято 4 электрона 5C-3H3-C0?C-1H+8KMnO4+12H2SO4®5C-3H3C+3OOH+5CO2+4K2SO4+8MnSO4+12H2O. C0-3e-®C+3 C-1-5e-®C+4 сумма отданных электронов 8 Mn+7+5e-®Mn+2
принято 5 электронов
Русская интерактивная дистанционная школа физики
|